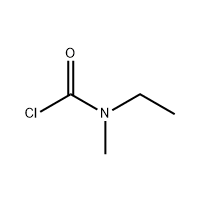
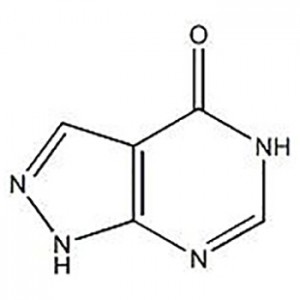
3'-amino-2'-hydroksi-[1,1'-bifenyyli]-3-karboksyylihappo
3'-amino-2'-hydroksi-[1,1'-bifenyyli]-3-karboksyylihappo
3'-amino-2'-hydroksi-[1,1'-bifenyyli]-3-karboksyylihappoa käytetään Eltrombopagin välituotteena.
Eltrombopag, jonka GlaxoSmithKline (GSK) on kehittänyt Isossa-Britanniassa ja kehitetty myöhemmin yhdessä Novartisin kanssa Sveitsissä, on ensimmäinen ja ainoa hyväksytty pienimolekyylinen peptiditön TPO-reseptoriagonisti maailmassa.USA:n FDA hyväksyi eltrombopagin vuonna 2008 idiopaattisen trombosytopeenisen purppuran (ITP) hoitoon ja vuonna 2014 vaikean aplastisen anemian (AA) hoitoon.Se on myös ensimmäinen lääke, jonka Yhdysvaltain FDA on hyväksynyt AA:n hoitoon viimeisten 30 vuoden aikana.
Joulukuussa 2012 Yhdysvaltain elintarvike- ja lääkevirasto hyväksyi Eltrombopagin trombosytopenian hoitoon kroonista hepatiitti C:tä (CHC) sairastavilla potilailla, jotta hepatiitti C -potilaat, joiden ennuste on huono alhaisen verihiutaleiden määrän vuoksi, voivat aloittaa ja ylläpitää interferonipohjaista maksasairauksien standardihoitoa.GlaxoSmithKline ilmoitti 3. helmikuuta 2014, että FDA myönsi Eltrombopagin läpimurtohoitolääkehyväksynnän hemopenian hoitoon potilailla, joilla on vaikea Chemicalbook aplastinen anemia (SAA), jotka eivät täysin vastanneet immuunihoitoon.USA:n FDA hyväksyi 24. elokuuta 2015 Eltrombopag-valmisteen trombosytopenian hoitoon aikuisilla ja 1-vuotiailla ja sitä vanhemmilla lapsilla, joilla on krooninen immuunitrombosytopenia (ITP), joilla ei ole riittävää vastetta kortikosteroideille, immunoglobuliineille tai pernan poistoon.4. tammikuuta 2018 Eltrombopag hyväksyttiin listattavaksi Kiinassa primaarisen immuunitrombosytopenian (ITP) hoitoon.


![3'-amino-2'-hydroksi-[1,1'-bifenyyli]-3-karboksyylihappo Esittelykuva](http://cdn.globalso.com/jindunchem-med/image351.png)
![3'-amino-2'-hydroksi-[1,1'-bifenyyli]-3-karboksyylihappo](http://cdn.globalso.com/jindunchem-med/image351-300x300.png)
![6-tetra-O-akteyyli-1-C-[4-kloori-3-[[4-[[(3S)-tetrahydrofuran-3-yyli]oksi]fenyyli]](http://cdn.globalso.com/jindunchem-med/0ecf55f0-300x300.jpg)